Klinische Studien
Temperaturüberwachungssysteme für jede Phase in klinischen Studien
Beim Versand von Studienmedikation darf es keine Unsicherheiten geben. Ob bei Sendungen mit unterschiedlichen Stabilitätsbudgets oder bei besonders empfindliche, personalisierte Arzneimittel und Therapien – Überwachungslösungen müssen Compliance, Rückverfolgbarkeit, Transparenz und Produktschutz gewährleisten.
- Qualifizierte Überwachungssysteme für Transport und Lagerung vor Ort
- Datenlogger für jede pharmazeutische Anwendung
- Real-Time-Alarme und Benachrichtigungen
- API-Integration für den nahtlosen Datentransfer zu Ihrer Clinical-Trial-Monitoring-Plattform
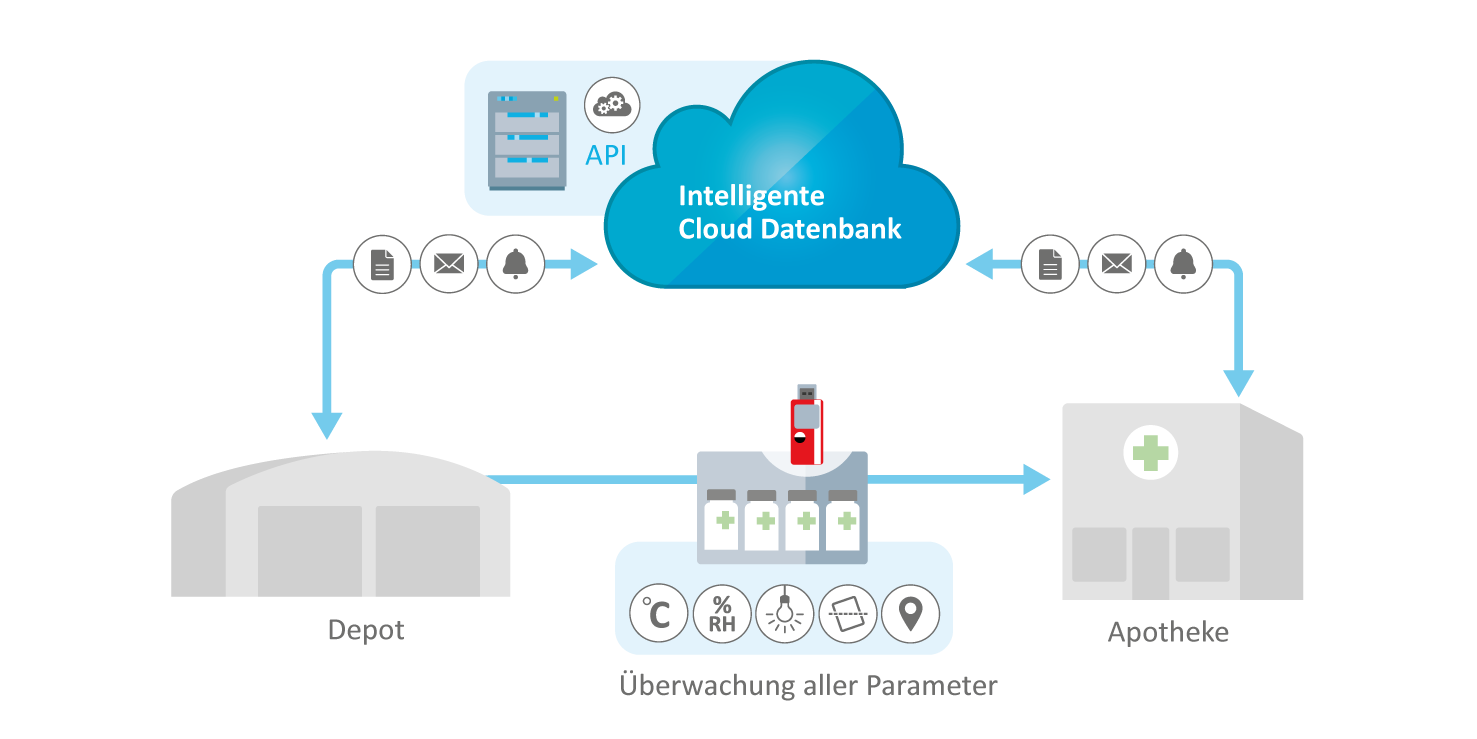
Überwachungsanwendungen im Rahmen klinischer Studien
ELPRO-qualifizierte Überwachungssysteme für klinische Studien schützen Bulk-Lieferungen während des Transports und stellen sicher, dass diese sicher und termingerecht an den Studienzentren ankommen.
Sie ermöglichen zudem eine präzise Überwachung der Lagerbedingungen vor Ort, um die Integrität und Qualität der Studienmedikation zu gewährleisten – und unterstützen gleichzeitig effiziente Direct-to-Patient-Lieferungen.
-
Überwachung während des Transports
-
Überwachung vor Ort
-
Direct-to-Patient

Bulk-Lieferungen an verschiedene Depots und Studienzentren
Arzneimittel für klinische Studien (IMPs) legen häufig einen komplexen Weg vom Hersteller bis zum Patienten zurück – meist über Lohnhersteller und regionale Depots in mehreren Ländern, bevor sie das Studienzentrum erreichen. Eine sorgfältige Planung dieser mehrstufigen Lieferkette ist entscheidend, um eine termingerechte Lieferung, die Produktintegrität und einen möglichst geringen Ausschuss sicherzustellen.
Ob weltweite Lieferungen mit unterschiedlichen Stabilitätsbudgets oder Zwischenlagerung in weltweit verteilten Depots – ELPRO schützt IMPs entlang der gesamten Lieferkette, überwacht die Umgebungsbedingungen und ermöglicht schnellere Freigaben durch kontinuierliche Real-Time-Daten, Real-Time-Prognosen, automatisierte Berichte und dynamisches Management der Stabilitätsbudgets.

Schutz der Stabilität von IMPs in Depots und Studienzentren
Die Temperaturüberwachung von Prüfpräparaten (IMPs) ist nicht nur während des Transports, sondern auch während der Lagerung in Depots und Studienzentren unerlässlich. Dies gilt insbesondere für empfindliche Produkte wie Impfstoffe, Insulin, Blutprodukte, Antibiotika, monoklonale Antikörper, Wachstumshormone, onkologische Arzneimittel, Augenmedikamente sowie personalisierte oder präzisionsmedizinische Therapien.
Die lückenlose Überwachung der Temperaturbereiche trägt dazu bei, die Stabilität und Wirksamkeit der IMPs zu erhalten, die Patientensicherheit zu gewährleisten und die ordnungsgemässe Handhabung zu dokumentieren – ein wesentlicher Bestandteil der Qualitätssicherung in klinischen Studien.

Transparenz vom Studienzentrum bis zum Patienten
Direct-to-Patient-Lieferungen gewinnen in klinischen Studien zunehmend an Bedeutung, um den Zugang zur Therapie zu erleichtern und die Patientenerfahrung zu verbessern. Gleichzeitig stellt die durchgängige Temperaturüberwachung entlang dieser erweiterten Lieferkette – vom Zentrallager bis ins Zuhause der Patienten – eine besondere Herausforderung dar.
Eine besonders effektive Lösung bietet der Einsatz von Indikatoren wie dem LIBERO ITS. Dieses elektronische, mehrstufige Temperaturüberwachungsgerät wird direkt am Prüfpräparate-Kit angebracht, überwacht kontinuierlich die Temperatur und berechnet das verbleibende Stabilitätsbudget – vom Verpacken bis zur Anwendung. Die einfache grün/rote LED-Anzeige ermöglicht es auch Laien, den Status des Produkts auf einen Blick zu erkennen und unterstützt so die sichere Anwendung und regelkonforme Lagerung über die gesamte Haltbarkeitsdauer von bis zu vier Jahren.
Lösungen für jede Phase der klinischen Studie
Hard- und Softwarelösungen von ELPRO sichern Qualität und Compliance in allen Phasen Ihrer klinischen Studie. Sie liefern schnelle, verlässliche und verwertbare Daten, die fundierte Entscheidungen ermöglichen, Real-Time-Transparenz schaffen, automatisierte Prozesse unterstützen und die regulatorische Compliance über alle Meilensteine der klinische Studie hinweg sicherstellen.
- Datenlogger (USB/PDF, Bluetooth®, Real-Time) für jede pharmazeutische Anwendung
- Intuitive Software mit übersichtlicher Datenvisualisierung
- Anpassbare Workflows
- Erweiterte Benutzer-/Zugriffsverwaltung
- Real-Time-Alarme und Benachrichtigungen
- Automatisierte Berichterstellung
- Automatische Bewertungen und softwarebasierte Alarmierung für Lieferungen mit unterschiedlichen Stabilitätsbudgets


Single-use USB
- Temperatur
- Automatische PDF-Berichterstellung
- Auslesung über USB-Anschluss

Cellular IoT Real-Time
- Temperatur, Feuchte, Position
- Real-Time-Datengenerierung und Alarmierung
- Single-use / Multi-use

Cellular IoT Real-Time
- °C, % rF
- LTE-M und NB-IoT (globales Roaming)
- IT-unabhängige Installation
- Problemlos skalierbar

Digitaler Indikator
- Visueller Alarm Status
- Dünn und selbstklebend an Einheiten
- LED Status für Go/No-Go Entscheidungen
Maximale Effizienz durch Automatisierung
Erfahren Sie, wie Lundbeck seine klinische und kommerzielle Lieferkette harmonisiert hat – durch die Weiterentwicklung einer ursprünglich für klinische Studien eingesetzten Überwachungslösung hin zu einem unternehmensweiten System für kommerzielle Prozesse.
liberoMANAGER hat Transparenz in unserem gesamten Unternehmen ermöglicht. Mit kritischen Temperaturdaten in der Cloud können unsere Lieferkettenteams an allen globalen Standorten auf die Informationen zugreifen, um Transporte zu validieren und fundierte Entscheidungen für die von ihnen gebuchten Strecken treffen. Wir können Probleme besser vorhersehen und begründete Entscheidungen treffen, um unsere Produkte zu schützen.
Integrierte Überwachung für CROs, CMOs und CDMOs
Mit den Umgebungsüberwachungslösungen von ELPRO optimieren Sie Ihre Prozesse, schützen kritische Daten für Ihre Kunden und verbessern Ihre Wirtschaftlichkeit. Entdecken Sie die Vorteile – und sprechen Sie uns an, um ein Pilotprojekt zu starten.
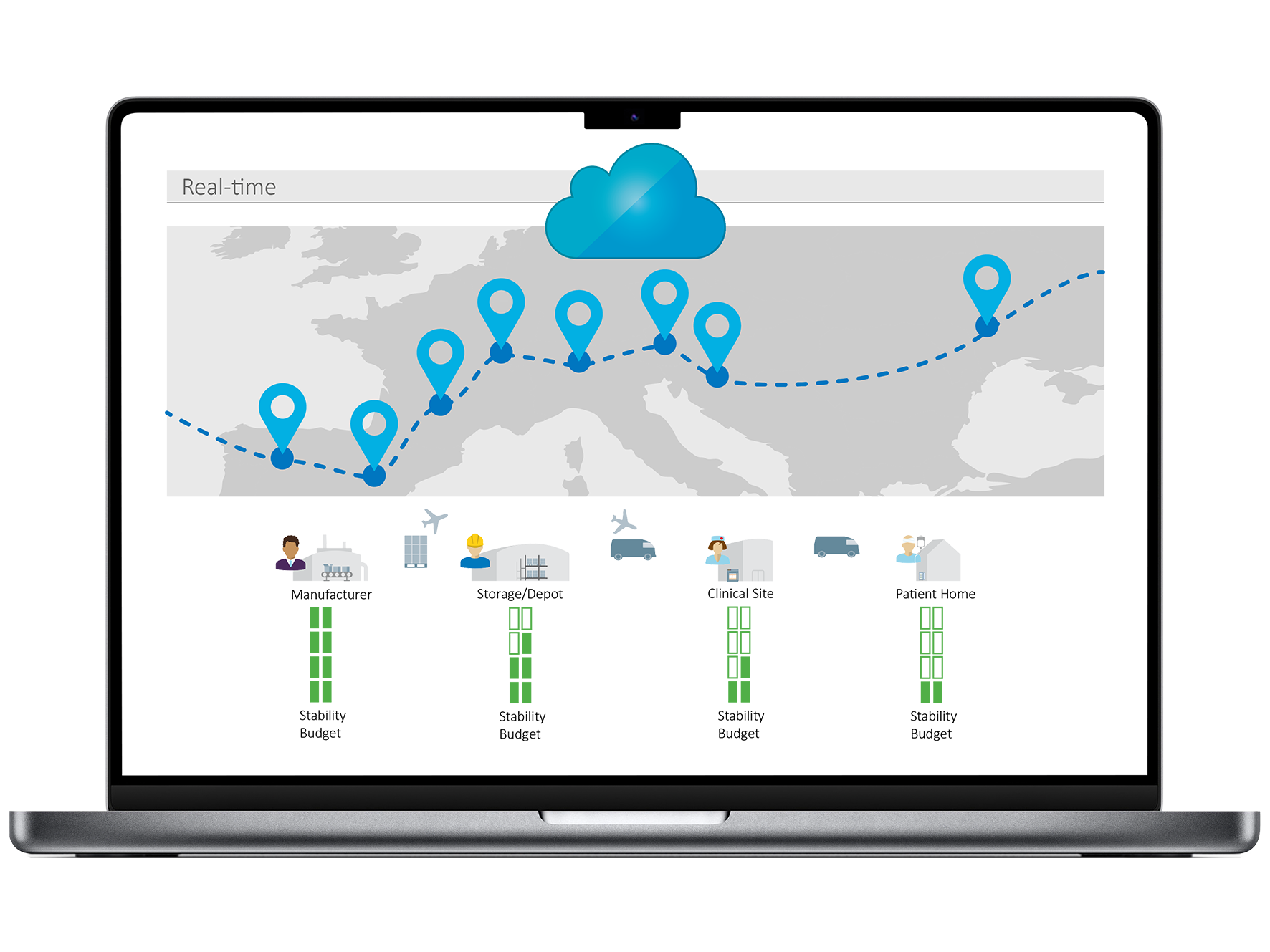
Optimierter Standortbetrieb
- Einfache Selbstinstallation für das Studienpersonal
- Keine aufwändigen Einrichtungsschritte
- Weniger Schulungsaufwand vor Ort
- Qualität verlässlich sicherstellen
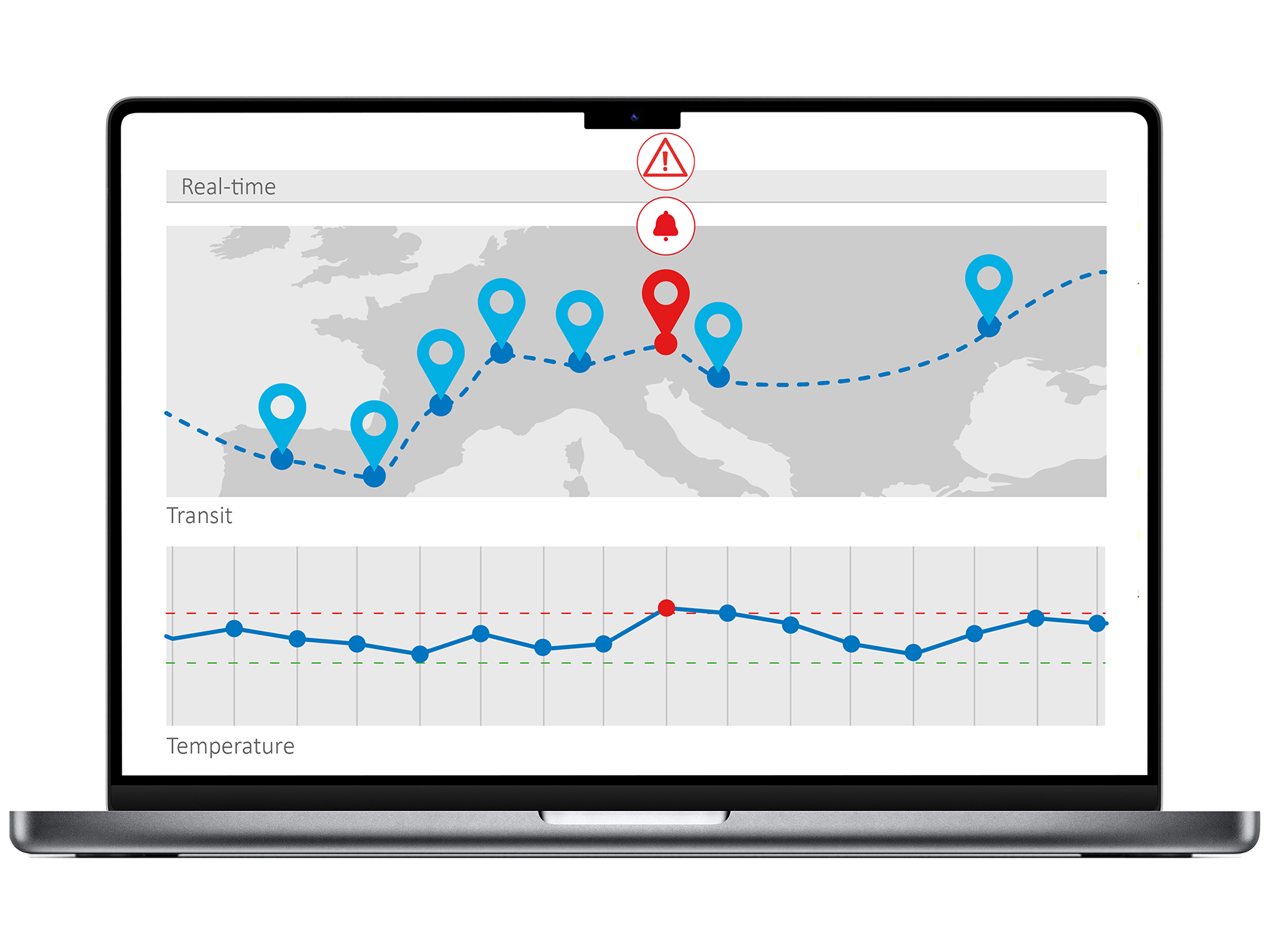
Qualitätssicherung stärken
- Zentrale Überwachung aller Lagereinheiten
- Sicherstellung der GMP-/GDP-Compliance
- Sofortige Alarmmeldungen bei Abweichungen
- Lückenlose, automatische Audit-Trails
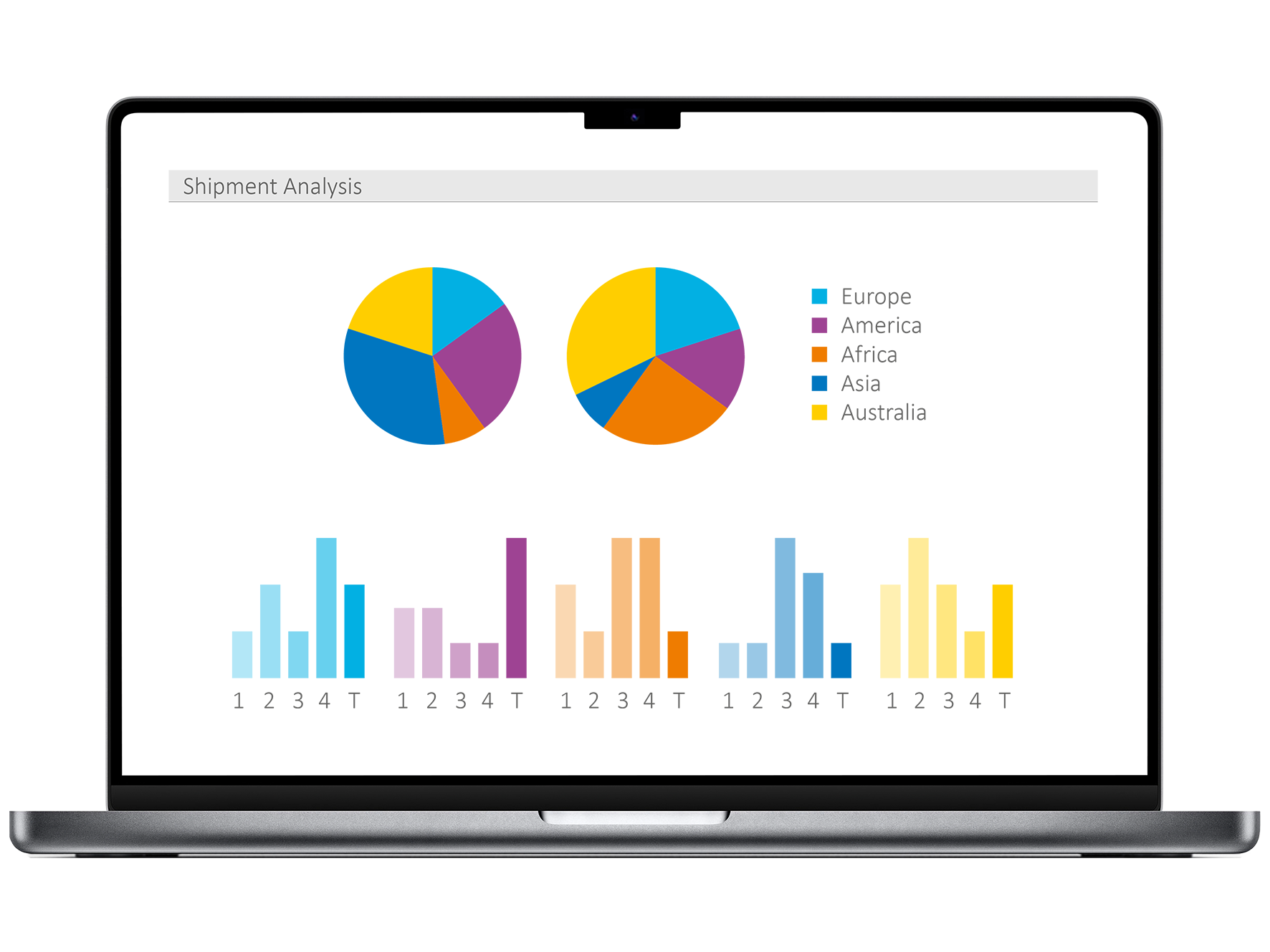
Volle Transparenz gewinnen
- Real-Time-Daten aus allen Standorten abrufen
- Sensoren- und Batteriestatus jederzeit verfolgen
- Individuelle Alarme und Analysen erhalten
- Benutzergruppen und Zugriffsrechte verwalten
Compliance leicht gemacht
Globale Vorschriften und Standards sind komplex – aber mit der notwendigen Expertise sind sie zu meistern. Mit umfassenden Lösungen sorgen wir dafür, dass Unternehmen die Compliance-Anforderungen erfüllen und für anstehende Audits gerüstet sind und weltweit jederzeit ein reibungsloser Betrieb gewährleistet ist. Wir kümmern uns um die Komplexität, damit Sie sich auf das Wesentliche konzentrieren können: Ihren Erfolg.

Sprechen wir über die Überwachung klinischer Studien. Kontaktieren Sie uns noch heute.

5 Fragen rund um die Überwachung des Versands bei klinischen Studien
Wie sieht es mit der Einhaltung gesetzlicher Vorschriften und dem Validierungsstatus aus?
Bei der Bewertung von Umgebungsüberwachungslösungen ist es entscheidend, den aktuellen Compliance-Status der Lösung in Bezug auf FDA 21 CFR Part 11, EU GMP Annex 11 und weitere relevante regulatorische Anforderungen zu hinterfragen. Zudem sollten Sie prüfen, ob der Anbieter eine Dokumentation über erfolgreiche Systemvalidierungen in vergleichbaren klinischen Studienumgebungen vorlegen kann.
Wichtige Aspekte:
- Sicherstellung der Datenintegrität und Auditfähigkeit
- Verifizierung, dass elektronische Aufzeichnungen und Unterschriften regulatorischen Vorgaben entsprechen
- Nachweis erfolgreicher Implementierungen in ähnlichen Anwendungsbereichen
- Verständnis der vorgelegten Validierungsdokumentation
- Erhalt der GMP/GLP-Compliance während der gesamten Studie
Ermöglicht die Lösung eine durchgängige Temperaturüberwachung?
Prüfen Sie die vollständigen End-to-End-Transparenzfunktionen, um eine kontinuierliche Temperaturüberwachung über alle kritischen Phasen hinweg sicherzustellen – vom Verpacken bis zur Auslieferung an den Patienten – und klären Sie die spezifischen Funktionen für jede einzelne Phase.
Wichtige Aspekte:
- Vermeidung von Lücken in der Temperaturüberwachung
- Empfang und Prüfung von Real-Time-Warnmeldungen
- Sicherstellung von Überwachungsgenauigkeit in jeder Phase
- Sicherung der Produktqualität entlang der gesamten klinischen Lieferkette
Wie ist das Datenmanagement und die Datenintegration geregelt?
Es ist unbedingt erforderlich, von Anfang an zu klären, wem die in einem System gespeicherten Daten gehören. Bei ELPRO bleiben Ihre Daten stets in Ihrem Besitz. Fragen Sie Ihren potenziellen Lösungsanbieter gezielt nach den Datenmanagement-Funktionen des Systems, einschließlich Datensicherheit, Backup-Verfahren sowie der Möglichkeit zur Integration in bestehende Clinical Trial Management Systeme (CTMS) und Qualitätsmanagementsysteme (QMS).
Wichtige Aspekte:
- Sicherstellung der Datenintegrität
- Gewährleistung eines ordnungsgemässen Audit-Trails für Compliance
- Zugriffsrechte und Berechtigungskonzepte
- Backup- und Wiederherstellungsverfahren
- Nahtlose Integration in CTMS-Systeme
Wie werden Alarme und Reaktionen auf Alarme geregelt?
Alarmmeldungen – lokal und remote – sind von grosser Bedeutung. Verzögerte Warnungen bei Temperatur- oder Feuchtigkeitsschwankungen und daraus resultierende verzögerte Reaktionen können den Verlust von wertvollen Lieferungen und Kits in Millionenhöhe verursachen, unwiederbringliche Forschungsergebnisse gefährden oder vielversprechende klinische Studien komplett zum Scheitern bringen. Klären Sie, wie das System mit Alarmmeldungen bei Temperatur- und Feuchtigkeitsexkursionen umgeht – einschliesslich Eskalationsprozessen, Benachrichtigungsmethoden und zugesicherter Reaktionszeiten.
Wichtige Aspekte:
- Unmittelbare Reaktion auf Abweichungen bei Temperatur und Feuchte
- Anpassungsmöglichkeiten von Alarmen
- Überprüfung verschiedener Benachrichtigungswege
- Einrichten von Eskalationsprozessen
Wie steht es um die Zuverlässigkeit und den Support des Systems?
Überprüfen Sie die Zuverlässigkeit der Umgebungsüberwachungslösung – inklusive Ausfallraten der Hardware, Batterielaufzeiten der Überwachungsgeräte sowie der Support-Struktur für Routine- und kritische Situationen.
Wichtige Aspekte:
- Sicherstellung einer durchgehenden Überwachung
- Backup-Systeme und Redundanzen
- Verfügbarkeit von Support und Reaktionszeiten
- Vermeidung von Datenlücken oder Systemausfälle
Weitere Aspekte, die es sich lohnt abzufragen
Weitere wichtige Aspekte bei der Überwachung Ihrer Studienmedikation und Forschungsprodukte:
- Detaillierte technische Spezifikationen
- Praxisbeispiele aus vergleichbaren Projekten
- Referenzen von anderen Organisationen im Bereich klinischer Studien
- Preisgestaltung und Analyse der Gesamtkosten
- Umsetzungszeitpläne und erforderliche Ressourcen
Newsletter-Anmeldung ELPRO News
ELPRO wird die in diesem Formular angegebenen Informationen dazu verwenden, mit Ihnen in Kontakt zu bleiben und Ihnen Updates sowie Marketing-Informationen per E-Mail zu übermitteln.


