GxP-Beratung, Qualifizierung und Services
GxP-Beratung, Qualifizierung und Services: mit ELPRO auf der sicheren Seite
Die Komplexität regulatorischer Anforderungen macht Compliance mühsam und zeitaufwändig. GxP-Beratungs- und Qualifizierungsservices im Bereich GxP-Compliance nehmen Ihnen diese Last ab und sorgen dafür, dass Sie gut auf anstehende Audits vorbereitet sind. Pharma-, Biotech- und Medizintechnikunternehmen sowie andere Organisationen aus dem Bereich der Biowissenschaften vertrauen auf fachkundige GxP-Compliance-Services, um das Risiko bei Inspektionen zu verringern, die Datenintegrität zu wahren und die konforme Produktentwicklung zu beschleunigen.
Die Services umfassen Räume und Lager, Geräte, Systeme und Flotten und beinhalten:
- Gerätequalifizierung
- Transportvalidierung und -verifizierung
- Lager- und Raumqualifizierung
- Systemvalidierung
-
GxP-Beratung
-
GxP-Qualifizierung & Validierung
-
GxP-Mappings

GxP-Beratung
Kunden profitieren von vier Jahrzehnten Erfahrung in der Kontrolle der Umgebungsbedingungen im Pharmaumfeld und der Compliance-Beratung. Die Berater von ELPRO bieten Schritt-für-Schritt-Unterstützung bei der Bewältigung komplexer Vorschriften, der Verbesserung von Prozessen, der Skalierung für zukünftiges Wachstum und der Entwicklung von Strategien zur Sicherstellung der Compliance, unabhängig von der Grösse des aktuellen Betriebs. Ganz gleich, ob Sie Ihr Qualitätsmanagementsystem (QMS) optimieren, Unterlagen für eine bevorstehende FDA- oder EMA-Inspektion vorbereiten oder skalierbare GxP-Compliance-Dienstleistungen einrichten müssen – die Berater von ELPRO liefern praktische, auditfähige Lösungen.

GxP-Qualifizierung und Validierung
Sorgfältige Qualifizierungsservices stellen sicher, dass Geräte und Umgebungsüberwachungssysteme den strengen GxP-Standards entsprechen. Es werden Risikobewertungen sowie DQ-, IQ-, OQ- und PQ-Dokumentationen bereitgestellt, die die Integrität der Betriebsabläufe gewährleisten und wertvolle Produkte schützen.
Das Angebot umfasst:
- Qualifizierung von Lager- und Transporteinheiten
- Validierung/Verifizierung von Transportprozessen
- Temperatur- und Feuchtigkeits-Mappings, einschliesslich Stresstests
- Erstellung individueller Qualifizierungs-/Validierungsdokumentationen

GxP-Temperatur- und Feuchtigkeits-Mappings
Genau Mappings der Umgebungsbedingungen sind entscheidend für die Einhaltung von GxP-Compliance. Die Services von ELPRO umfassen detaillierte Mappings der Umgebungsparameter, insbesondere der Temperatur und der relativen Luftfeuchtigkeit, und gewährleisten so die Produktqualität und die Einhaltung gesetzlicher Vorschriften. Dazu gehören:
- Lager- oder Reinräume
- Container
- Thermische Verpackungen oder Boxen
- Kühl-, Tiefkühlschränke oder ULT
- LKW, Vans oder gesamte Fuhrpark
- Lane Studies
Sie haben die Wahl zwischen Vor-Ort- oder Remote-Mappings sowie Self-Service-Mappingkits.
Vom Temperatur-Mapping zur Behördenfreigabe in 2 Monaten
Lesen Sie mehr über die erfolgreiche Durchführung eines GMP-konformen Temperatur-Mappings im hochautomatisierten AutoStore-Lager einer der führenden Online-Apotheken Deutschlands. Erhalten Sie Einblicke in die Herausforderungen, den Prozess und die Ergebnisse.
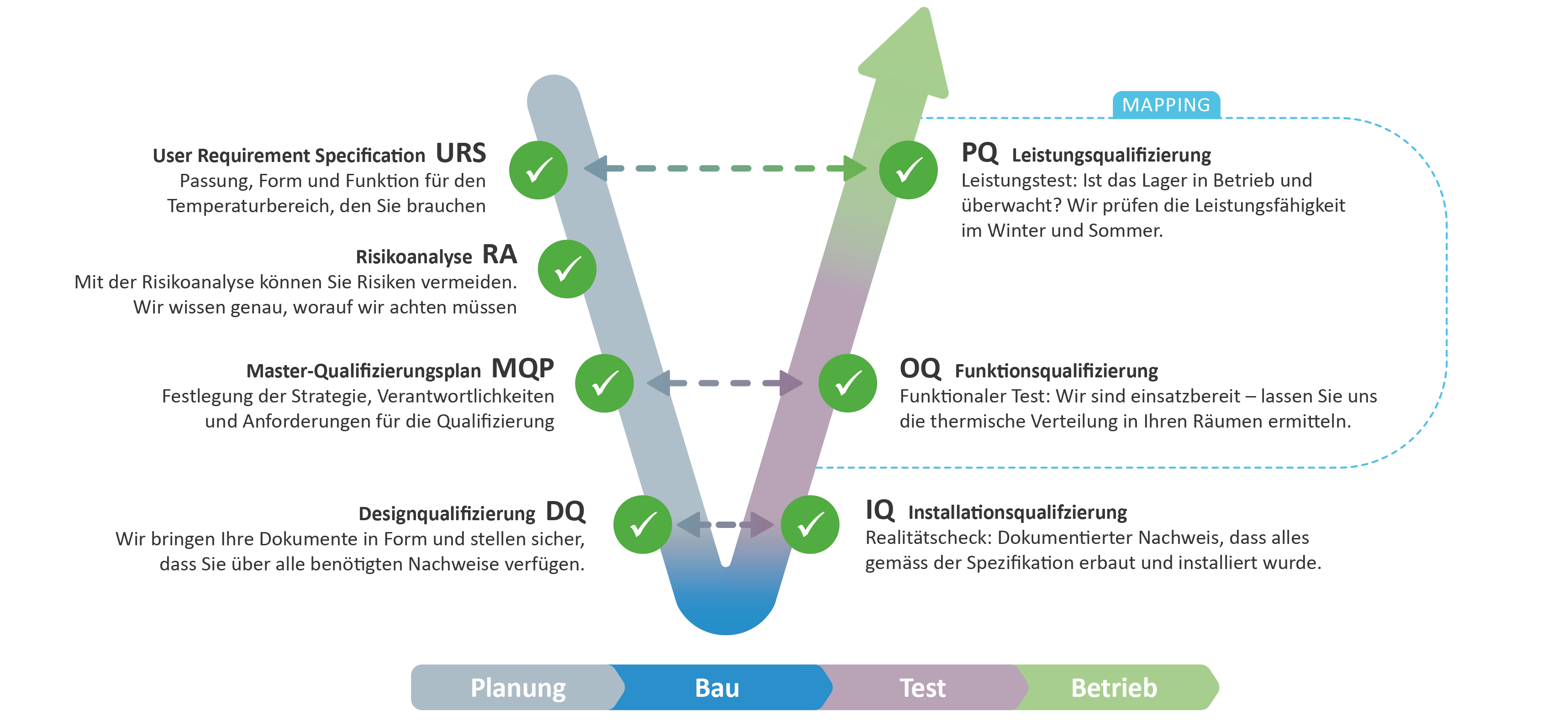
Das V-Modell immer im Blick
Das V-Modell ebnet Ihnen den Weg zu lückenloser Compliance. Sie entscheiden, in welcher Phase Sie unser Expertenwissen für Ihre GxP-Compliance nutzen möchten.
Risikobasierte GxP-Services und Qualifizierung für Überwachungssysteme
Ein risikobasierter Ansatz ist für eine effektive GxP-Compliance-Beratung von grundlegender Bedeutung. ELPRO wendet strukturierte Risikomethoden an, um für jedes Qualifizierungs- und Validierungsprojekt den geeigneten Umfang, die erforderliche Tiefe und die Dokumentationsanforderungen zu definieren.
- Strukturierte Risikobewertungen zur Festlegung des Qualifizierungsumfangs und der Validierungstiefe, um sicherzustellen, dass Ressourcen dort eingesetzt werden, wo sie für die Compliance am wichtigsten sind
- Identifizierung kritischer Parameter und Systemkomponenten, die sich auf die Compliance auswirken, von Temperatursensoren und Datenloggern bis hin zu Software-Schnittstellen und Alarmsystemen
- Dokumentation, die den regulatorischen Erwartungen und der Vorbereitung für Inspektionen entspricht, einschliesslich Risikobewertungsberichten, Qualifizierungsprotokollen (IQ/OQ/PQ) und Zusammenfassungsberichten, die den Anforderungen der Prüfer von FDA, EMA und WHO genügen
Lebenszyklusansatz für GxP-Services und die Qualifizierung von Überwachungssystemen
Compliance ist kein einmaliger Vorgang. Sie erfordert einen disziplinierten Lebenszyklusansatz. Die GxP-Compliance-Services von ELPRO sind darauf ausgelegt, Ihre Überwachungssysteme vom ersten Entwurf bis zum laufenden Betrieb zu unterstützen und so die kontinuierliche Einhaltung der Vorschriften sicherzustellen.
- End-to-End-Qualifizierungsstrategie vom Systemdesign über den Betrieb bis hin zur Wartung, abgestimmt auf das V-Modell-Framework und aktuelle regulatorische Anforderungen
- Regelmässige Überprüfung und Requalifizierung zur Gewährleistung der fortlaufenden Compliance bei Änderungen von Vorschriften, Anlagenbedingungen oder betrieblichen Anforderungen
- Unterstützung bei der Änderungskontrolle zur Verwaltung von Systemaktualisierungen in regulierten Umgebungen, um sicherzustellen, dass Hardware-Upgrades, Softwareänderungen oder Anlagenmodifikationen ordnungsgemäss bewertet und in Ihrem QMS dokumentiert werden
Halten Sie Ihr Umgebungsüberwachungssystem konform
Weltweit vertrauen Logistik- und Biopharmaunternehmen sowie solche, die klinische Studien durchführen, auf GxP-Service-Experten von ELPRO.
500+
Lagerhäuser qualifiziert
10,000+
Temperatur-Mappings in Einrichtungen
20,000+
Kalibrierungen jährlich
ELPRO erleichterte die Qualifizierung der Temperatur-Monitoringgeräte und unserer Kühlhäuserdurch exzellentes Fachwissen und bedarfsorientierte technische Unterstützung
Unsere Zusammenarbeit mit ELPRO bei der Qualifizierung und beim Mapping unseres neuen GMP/GDP-konformen Lagers war sehr erfolgreich. Alle Schritte bis zur behördlichen Inspektion wurden professionell begleitet. Letztendlich hatten wir keinerlei Mängel.
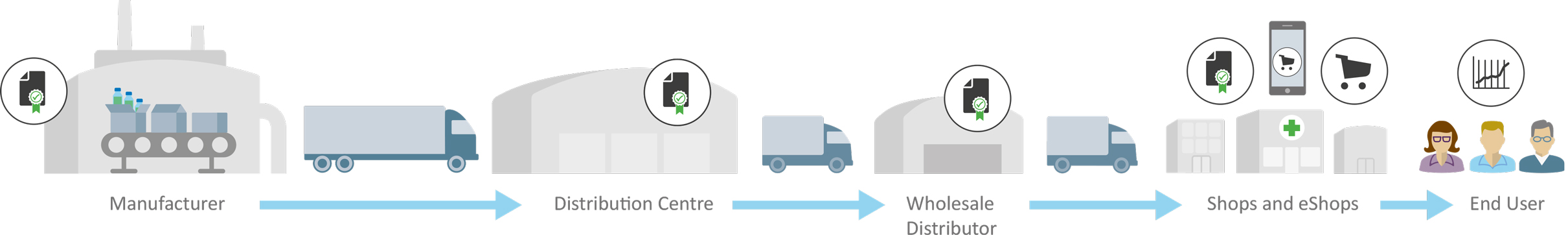
Unübertroffener GxP-Support für Ihre gesamte Lieferkette
GxP-Services müssen die gesamte Lieferkette unterstützen, um eine kontinuierliche Temperaturkontrolle und Compliance zu gewährleisten:
- Massgeschneiderte Lösungen überwachen den kritischen Temperaturbereich für lebensrettende, temperaturempfindliche Produkte aufrecht.
- Cloud-basierte Lösungen bieten Echtzeitüberwachung und Dateneinblicke für eine nahtlose Nachverfolgung.
- Experten minimieren Compliance-Risiken und gewährleisten Produktsicherheit und Compliance von der Lagerung bis zum Vertrieb.
Compliance leicht gemacht
Globale Vorschriften und Standards sind komplex – aber mit der notwendigen Expertise sind sie zu meistern. Mit umfassenden Lösungen sorgen wir dafür, dass Unternehmen die Compliance-Anforderungen erfüllen und für anstehende Audits gerüstet sind und weltweit jederzeit ein reibungsloser Betrieb gewährleistet ist. Wir kümmern uns um die Komplexität, damit Sie sich auf das Wesentliche konzentrieren können: Ihren Erfolg.

Sprechen wir über GxP. Nehmen Sie Kontakt mit uns auf.

Häufige Fragen zu GxP-Services, GxP-Beratung und Qualifizierung
Wofür steht GxP?
GxP steht für „Good x Practice“, wobei das „x“ für verschiedene Bereiche wie Herstellung (GMP), Labor (GLP) und Vertrieb (GDP) steht. Es handelt sich um einen Oberbegriff für Vorschriften und Richtlinien, die Qualität, Sicherheit und Compliance in Branchen wie Pharmazie, Biotechnologie und Healthcare gewährleisten..
Einige gängige GxP-Standards sind:
- GMP (Good Manufacturing Practice) – Gewährleistet, dass Produkte durchgängig nach Qualitätsstandards hergestellt und kontrolliert werden.
- GLP (Good Laboratory Practice) – Gewährleistet die Zuverlässigkeit und Integrität von Laborstudien.
- GDP (Good Distribution Practice) – Gewährleistet die ordnungsgemässe Handhabung, Lagerung und den Transport von pharmazeutischen Produkten.
- GCP (Good Clinical Practice) – Gewährleistet die ethische Durchführung, Sicherheit und Zuverlässigkeit klinischer Studien und schützt gleichzeitig die Rechte und das Wohlergehen der Teilnehmer.
Diese Richtlinien tragen dazu bei, die Produktqualität, die Einhaltung gesetzlicher Vorschriften und die Patientensicherheit zu gewährleisten.
Was ist ein GxP-validiertes System?
Ein GxP-validiertes System ist ein computergestütztes System, das getestet und dokumentiert wurde, um sicherzustellen, dass es die regulatorischen Anforderungen an Datenintegrität, Genauigkeit, Zuverlässigkeit und Sicherheit in GxP-Umgebungen (wie GMP, GLP oder GDP) erfüllt. Die wichtigsten Aspekte eines GxP-validierten Systems sind:
- Einhaltung von Vorschriften – Das System muss gesetzliche Anforderungen wie FDA 21 CFR Part 11, EU Annex 11 und andere branchenspezifische Richtlinien erfüllen.
- Validierungsprozess (CSV – Computerized System Validation) – Das System durchläuft eine Installationsqualifizierung (IQ), eine Funktionsqualifizierung (OQ) und eine Leistungsqualifizierung (PQ), um sicherzustellen, dass es wie vorgesehen funktioniert.
- Datenintegrität (ALCOA+-Prinzipien) – Stellt sicher, dass Daten zuordenbar, lesbar, zeitnah, original, genau und vollständig, konsistent, dauerhaft und verfügbar sind.
- Audit-Trail und Sicherheit – Das System muss alle Änderungen verfolgen, die Benutzerzugriffskontrolle sicherstellen und unbefugte Änderungen verhindern.
-
Dokumentierte Nachweise – Die Validierung muss vollständig dokumentiert werden, um die Konformität bei Audits und Inspektionen nachweisen zu können. Diese Dokumentation umfasst in der Regel einen Validierungsplan, IQ-/OQ-/PQ-Protokolle und Durchführungsberichte, eine Rückverfolgbarkeitsmatrix sowie einen abschliessenden Validation Summary Report.
Was sind die regulatorischen Anforderungen von GxP?
GxP-Vorschriften sind Richtlinien und Standards, die die Produktqualität, Sicherheit und Datenintegrität in Branchen wie der Pharma, Biotechnologie und Healthcare währleisten. Diese Vorschriften variieren je nach Region und Anwendung, basieren jedoch auf gemeinsamen Grundsätzen. Die wichtigsten GxP-Vorschriften sind:
1. Vorschriften für Herstellung und Laboratorien
- EU-GMP-Leitlinien (EudraLex Band 4)
- US-FDA 21 CFR Part 210 und 211
- WHO-Leitlinien
- OECD-Grundsätze der GLP
- US-FDA 21 CFR Part 58
2. Vorschriften für Vertrieb und Lieferkette
- EU-GDP-Leitlinien (2013/C 343/01)
- US-FDA-GDP-Leitlinien für die Industrie
- WHO-Leitlinien
-
ISPE Good Practice Guide
3. Vorschriften zur Datenintegrität und elektronischen Aufzeichnungen
- FDA 21 CFR Part 11 – Legt Anforderungen für elektronische Aufzeichnungen und Signaturen fest, um die Datenintegrität sicherzustellen.
- EU Annex 11 – Bezieht sich auf computergestützte Systeme in GxP-Umgebungen.
- MHRA- und WHO-Richtlinien zur Datenintegrität – Betonen die Einhaltung der ALCOA+-Prinzipien (Attributable, Legible, Contemporaneous, Original, Accurate, plus Complete, Consistent, Enduring, Available).
4. Vorschriften für Medizinprodukte und klinische Studien
- ISO 13485 – Qualitätsmanagementsystem für Medizinprodukte.
- ICH GCP (Good Clinical Practice) Leitlinien – Gewährleistet ethische und wissenschaftliche Standards in klinischen Studien.
Was sind typische GxP-Services?
Typische GxP-Services gewährleisten die Einhaltung gesetzlicher Standards in Branchen wie Pharmazie, Biotechnologie und Healthcare. Diese Services umfassen:
1. Qualifizierungs- und Validierungsservices
- Spezifikation der Benutzeranforderungen (URS)
- Risikobewertung
- Temperatur-Mappings – Sicherstellung, dass kontrollierte Umgebungen (z. B. Lagerhäuser, Kühlschränke, Gefrierschränke) die GxP-Anforderungen erfüllen.
- Gerätequalifizierung (IQ/OQ/PQ) – Installations-, Funktions- und Leistungsqualifizierung von Überwachungs- und Speichersystemen.
2. Überwachungs- und Compliance-Lösungen
- Umgebungsüberwachung (Temperatur, Luftfeuchtigkeit, CO₂ usw.) – Kontinuierliche Überwachung der Lager- und Transportbedingungen.
- Abweichungsmanagement und Umgang mit Alarmen – Sicherstellung einer zeitnahen Reaktion auf Bedingungen, die ausserhalb der Spezifikationen liegen.
- Audit Trail und Datenintegritätssicherung – Sichere Datenprotokollierung und Dokumentation zur Einhaltung der Vorschriften.
3. GxP-Beratung und Audits
- Unterstützung bei der Einhaltung gesetzlicher Vorschriften – Beratung zu GMP, GDP und anderen GxP-Anforderungen. Dazu gehören Gap-Analysen im Hinblick auf aktuelle regulatorische Anforderungen, die Korrektur von Qualitätssystemen sowie die Erstellung der erforderlichen Dokumentation wie Standardarbeitsanweisungen (SOPs), Qualifizierungsprotokolle und Validierungsberichte.
- Risikobewertungen und Schwachstellenanalysen – Identifizierung potenzieller Compliance-Risiken und Verbesserungsmöglichkeiten.
- Vorbereitung auf Audits und Inspektionen – Vorbereitung auf behördliche Inspektionen (z. B. FDA, EMA).
4. Schulungen und Dokumentation
- GxP-Schulungen für Mitarbeiter – Schulung der Mitarbeiter zu regulatorischen Anforderungen und Best Practices.
- Entwicklung von Standardarbeitsanweisungen (SOPs) – Erstellung dokumentierter Richtlinien zur Einhaltung der Vorschriften. Zu den weiteren GxP-Dokumentationsservices gehören die Erstellung oder Überprüfung von Chargenprotokollen, Qualifizierungsprotokollen, Validierungsplänen, Verfahren zur Änderungskontrolle sowie der Dokumentation von Abweichungen und Korrigierenden und Vorbeugenden Massnahmen (CAPA) zur Unterstützung eines robusten Qualitätsmanagementsystems (QMS).
Diese Services helfen Unternehmen dabei, Compliance zu gewährleisten, Produktqualität sicherzustellen und Patientensicherheit zu gewährleisten.
Welche drei Elemente sind für GxP relevant?
Die drei Grundsätze von GxP sind:
- Rückverfolgbarkeit – Die Möglichkeit, die Entwicklung, Herstellung, Prüfung und den Vertrieb eines Produkts zu verfolgen, um Transparenz und Nachvollziehbarkeit zu gewährleisten.
- Verantwortlichkeit – Klare Definition von Verantwortlichkeiten und Dokumentation von Massnahmen, um die Einhaltung von Vorschriften und Standards sicherzustellen.
- Datenintegrität – Sicherstellung, dass Daten während ihres gesamten Lebenszyklus korrekt, vollständig, konsistent und sicher sind, um die Einhaltung gesetzlicher Vorschriften und die Entscheidungsfindung zu unterstützen.
Diese Grundsätze tragen dazu bei, Produktqualität, Compliance und Patientensicherheit in Branchen wie der Pharmaindustrie und dem Gesundheitswesen aufrechtzuerhalten.
Welche Rolle spielt das V-Modell bei der Qualifizierung?
Das V-Modell ist ein strukturierter Ansatz, der bei der GxP-Qualifizierung und -Validierung verwendet wird, um sicherzustellen, dass Geräte, Einrichtungen und computergestützte Systeme den gesetzlichen Anforderungen entsprechen. Es wird häufig in den Bereichen Good Manufacturing Practice (GMP), Good Laboratory Practice (GLP) und Good Distribution Practice (GDP) angewendet.
Das V-Modell folgt einer „V“-Form, wobei:
- die linke Seite die Anforderungen und das Design definiert,
- die rechte Seite das System anhand dieser Anforderungen überprüft und validiert und
- die Mitte (Implementierungsphase) die Installation und Konfiguration des Systems darstellt.
Jeder Schritt auf der linken Seite hat eine entsprechende Testphase auf der rechten Seite, wodurch vollständige Rückverfolgbarkeit und Konformität gewährleistet sind.
Was sind die 5 R's der Risikobewertung?
Die 5 R's der Risikobewertung bieten einen strukturierten Ansatz zur effektiven Identifizierung und zum Management von Risiken. Sie helfen Unternehmen, insbesondere in regulierten Branchen wie der Pharmaindustrie, die Compliance aufrechtzuerhalten und potenzielle Ausfälle zu minimieren. Die Anwendung der 5 R's gewährleistet einen proaktiven und systematischen Ansatz für das Risikomanagement in stark regulierten Umgebungen.
- Recognize (Erkennen) – Identifizieren Sie potenzielle Risiken, die sich auf die Produktqualität, die Patientensicherheit oder die Compliance auswirken könnten. Dazu gehört die Analyse von Prozessen, Anlagen und Schwachstellen in der Datenintegrität.
- Rank (Einstufen) – Bewerten und priorisieren Sie Risiken anhand ihrer Wahrscheinlichkeit, Schwere und Erkennbarkeit. Methoden wie FMEA (Failure Modes and Effects Analysis) helfen dabei, zu bestimmen, welche Risiken sofortige Massnahmen erfordern.
- Respond (Reagieren) – Entwickeln und implementieren Sie Massnahmen zur Risikokontrolle, wie z. B. Prozessverbesserungen, Schulungen, Systemvalidierungen oder zusätzliche Überwachungsmassnahmen, um Risiken zu beseitigen oder zu mindern.
- Record (Aufzeichnen) – Dokumentieren Sie Risikobewertungen, Strategien zur Risikominderung und Korrekturmassnahmen, um die Einhaltung von GxP-Vorschriften wie CFR 21 Part 11, ICH Q9 und ISO 14971 sicherzustellen.
- Review (Überwachen) – Überwachen Sie Risiken kontinuierlich und aktualisieren Sie Bewertungen, um Änderungen in Prozessen, Vorschriften oder neuen Gefahren Rechnung zu tragen. Regelmässige Überprüfungen gewährleisten langfristige Compliance und Betriebssicherheit.
Was ist der Unterschied zwischen CSV und GxP?
GxP ist ein weit gefasster Begriff, der alle „Good Practice“-Vorschriften – GMP, GLP, GDP, GCP und andere – umfasst, die regeln, wie Unternehmen der Life-Sciences-Branche ihre Produkte und Prozesse entwickeln, herstellen, vertreiben und dokumentieren. CSV (Computerized System Validation) ist eine spezifische Massnahme, die im Rahmen von GxP durchgeführt wird, um nachzuweisen, dass ein computergestütztes System stets wie vorgesehen funktioniert.
Praktisch gesehen definiert GxP die regulatorischen Anforderungen; CSV ist der dokumentierte Prozess zur Erfüllung dieser Anforderungen für Software und IT-Systeme. CSV folgt einem strukturierten Lebenszyklus – einschliesslich Lastenheft (URS), Risikobewertung und IQ/OQ/PQ-Tests – und liefert die dokumentierten Nachweise, die erforderlich sind, um die Aufsichtsbehörden davon zu überzeugen, dass ein System für den beabsichtigten GxP-Einsatz geeignet ist. Für Biotech-Unternehmen und andere Organisationen im Bereich der Biowissenschaften ist die Integration von CSV in Ihr QMS unerlässlich, um sowohl die Zuverlässigkeit des Systems als auch die kontinuierliche Einhaltung der regulatorischen Anforderungen sicherzustellen.
Welche Dokumentation ist für GxP-Services und die Qualifizierung von Umgebungsüberwachungssystemen erforderlich?
Ordnungsgemässe GxP-Dokumentationsservices sind entscheidend, um bei behördlichen Inspektionen Compliance nachzuweisen. Für die Qualifizierung von Umgebungsüberwachungssystemen sind in der Regel folgende Dokumente erforderlich:
-
Validierungs-Masterplan (VMP) oder Qualifizierungsplan – Definiert die Gesamtstrategie, den Umfang und die Verantwortlichkeiten für das Qualifizierungsprojekt.
-
Lastenheft (URS) – Beschreibt, was das System aus Sicht der Anwender und der Aufsichtsbehörden leisten muss.
-
Risikobewertung – Identifiziert und priorisiert kritische Systemkomponenten und -parameter.
-
Protokoll und Bericht zur Installationsqualifizierung (IQ) – Überprüft, ob das System gemäss den Herstellerspezifikationen und Standortanforderungen korrekt installiert wurde.
-
Protokoll und Bericht zur Betriebsqualifizierung (OQ) – Bestätigt, dass das System innerhalb seines definierten Betriebsbereichs wie vorgesehen funktioniert.
-
Protokoll und Bericht zur Leistungsqualifizierung (PQ) – Weist eine konsistente Systemleistung unter realen Betriebsbedingungen nach.
-
Temperaturmessbericht – Dokumentiert die räumliche Temperaturverteilung innerhalb einer überwachten Umgebung.
-
Kalibrierzertifikate – Nachweis, dass Sensoren und Messgeräte die erforderlichen Messgenauigkeitsstandards erfüllen.
-
Rückverfolgbarkeitsmatrix – Verknüpft jede Benutzeranforderung mit einem entsprechenden Test und gewährleistet so eine vollständige Abdeckung.
-
Validierungszusammenfassungsbericht – Fasst alle Qualifizierungsaktivitäten zusammen und schliesst den Validierungszyklus formell ab.
-
Standardarbeitsanweisungen (SOPs) – Dokumentierte Verfahren für den Systembetrieb, die Alarmreaktion, den Umgang mit Abweichungen und die regelmässige Überprüfung.
Wie lange dauert ein typischer GxP-Qualifizierungsprozess für Umgebungsüberwachungssysteme?
Der Zeitrahmen für die GxP-Qualifizierung eines Umgebungsüberwachungssystems variiert je nach Umfang, Komplexität und aktuellem Stand der Dokumentation. Als allgemeine Richtlinie gilt:
- Kleine oder Einzelraum-Qualifizierungen (z. B. ein einzelner Kühlraum oder ein Labor): 2–6 Wochen, einschliesslich Dokumentation, Mapping und Berichterstellung.
- Projekte mittleren Umfangs (z. B. ein GDP-Lager mit mehreren Zonen oder eine klinische Lagereinrichtung): 6–12 Wochen, unter Berücksichtigung der Risikobewertung, der vollständigen Durchführung von IQ/OQ/PQ sowie der behördlichen Prüfzyklen.
- Grosse oder komplexe Umgebungen (z. B. ein hochautomatisiertes Distributionszentrum oder eine Einführung an mehreren Standorten): 3–6 Monate oder länger, insbesondere wenn die Integration in das Qualitätsmanagementsystem (QMS), die Änderungskontrolle und die Vorbereitung auf behördliche Inspektionen einbezogen werden.
Die Zeitpläne können verkürzt werden, wenn die vorhandene Dokumentation gut organisiert ist und eine klare Qualifizierungsstrategie vorliegt. Das GxP-Compliance-Beratungsteam von ELPRO arbeitet von Anfang an mit Ihren Qualitäts- und Betriebsteams zusammen, um Projekte genau zu definieren, Ressourcen effizient zuzuweisen und Ihre Audit- oder Inbetriebnahme-Fristen einzuhalten.
Newsletter-Anmeldung ELPRO News
ELPRO wird die in diesem Formular angegebenen Informationen dazu verwenden, mit Ihnen in Kontakt zu bleiben und Ihnen Updates sowie Marketing-Informationen per E-Mail zu übermitteln.


